细胞产生的力在广泛的生物过程中起着至关重要的作用,例如细胞运动、胞质分裂和组织形态发生。在NatureCommunications发表的一项研究中,由日本国立基础生物学研究所定量生物学部领导的研究小组成功开发了“OptoMYPT”:一种利用聚焦光降低肌动蛋白和肌球蛋白收缩力的光遗传学工具.
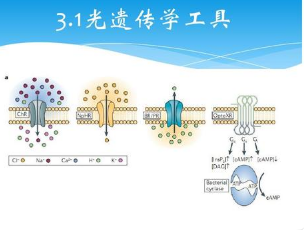
研究人员设计了一种光遗传学工具来直接灭活非肌肉肌球蛋白II,它与肌动蛋白丝协同产生细胞收缩力。为了实现这一目标,他们专注于MYPT1,这是一种肌球蛋白失活所需的蛋白质,一种使磷酸酶PP1c靠近磷酸化肌球蛋白的蛋白质。这随后导致肌球蛋白去磷酸化和失活。利用这一特性,研究人员旨在通过使用MYPT1的PP1c结合域(PP1BD)来光学操纵最初存在于细胞中的PP1c的定位。
为了开发OptoMYPT,我们使用了一种称为iLID的工具来控制蛋白质的光定位。该工具基于蓝光照射导致iLID蛋白与SspB蛋白结合的想法。首先,iLID蛋白定位于细胞膜,而与MYPT1的PP1BD融合的SspB在细胞质内表达。然后,蓝光照射通过与iLID结合,诱导SspB-PP1BD从细胞质向膜的易位,导致内源性PP1c向膜的共同募集。最后,膜招募的PP1c使细胞膜附近的肌球蛋白去磷酸化并失活。”
为了了解细胞分裂的机制,研究小组将他们的OptoMYPT应用于分裂细胞。当将蓝光照射在分裂细胞的两极以减弱细胞皮层产生的张力时,细胞分裂沟的进入速度加快。此外,当细胞皮层的张力仅在一侧减弱时,两个子细胞之间会发生振荡的细胞质流动。因此,通过使用OptoMYPT施加局部力扰动,研究小组证明了细胞表面产生的力的最佳强度和对称性对于细胞分裂的正常进程至关重要。
“我们相信这个工具OptoMYPT将有助于理解涉及肌动球蛋白细胞骨架的各种胚胎学和细胞生物学现象,”研究小组成员KazuhiroAoki教授说。他补充说:“未来,我们希望它可以用于自由设计细胞和组织的形状以及形成人造器官。”
标签:
版权声明:本文由用户上传,如有侵权请联系删除!
